Газы, применяемые в производстве источников света, разделяются на технологические и топливные.
а) Технологические газы. Назначение и область применения.
К технологическим газам относятся водород, азот, кислород и инертные газы — аргон, неон, гелий, криптон, ксенон, а также их смеси.
Технологические газы применяют для наполнения газоразрядных источников света и ламп накаливания и создания восстановительной, окислительной или защитной (инертной) среды на многих технологических операциях.
Для наполнения ламп в основном используются инертные газы и их смеси. При этом они выполняют в лампах роль светоизлучающей среды (газосветные трубки, газовые импульсные лампы и др.), среды, замедляющей испарение вольфрама (лампы накаливания), среды, облегчающей зажигание разряда в лампе, предотвращающей быстрое разрушение катода (люминесцентные лампы, лампы ДРЛ и др.).
Водород используется в основном при термической обработке изделий для создания защитной и восстановительной атмосферы, для получения высокой температуры пламени газовых горелок при обработке тугоплавких стекол и др.
Кислород применяется в основном для повышения тем пературы пламени газовых горелок, создания окислительной среды на некоторых технологических операциях, а также для наполнения некоторых источников света (лампы- фотовспышки).
Азот служит для создания защитной среды на технологических операциях, восстановительной среды в смеси с водородом (препарировочный газ), промывки ламп во время вакуумной обработки на откачных установках (автоматах) и наполнения ламп в смеси с инертными газами, для получения аммиака и др.
Свойства технологических газов.
Многие свойства газов не остаются постоянными при изменении давления. При больших давлениях для газов характерны: высокая теплопроводность и ее независимость от давления в широких пределах, наличие конвекции, медленное протекание процесса диффузии, трение между слоями газа при его движении по трубам, зависимость пропускной способности газопровода от давления.
При низких давлениях, т. е. в условиях высокого вакуума, для газов характерны: низкая теплопроводность и ее зависимость от давления, отсутствие конвекции, почти мгновенное протекание процесса диффузии, отсутствие внутреннего трения, независимость пропускной способности газопровода от давления. С увеличением давления температура газа повышается, а с уменьшением — падает.
Условно различают понятия «пар» и «газ». Паром называют газообразное вещество при температуре ниже критической, а газом — при температуре выше критической. Критической называют ту температуру, выше которой вещество может находиться только в газообразном состоянии и ни при каком давлении не может быть обращено в жидкость. Переход многих обычных газов в состояние пара и их последующая конденсация широко используется как в производстве самих газов (сжижение воздуха), так и при отпайке ламп с давлением наполняющего газа выше атмосферного, а также для других целей.
Важным свойством любого газа является его способность поглощаться твердыми телами и выделяться из них. Поглощение газов твердыми телами происходит как их поверхностью (адсорбция), так и объемом (абсорбция). Твердое тело способно поглощать значительные объемы газа, иногда во много раз превышающие его собственный объем. Газ, поглощаясь твердым телом, сжимается и уплотняется в нем. Это используется в газопоглотителях (геттерах).
При нагреве твердого тела обычно происходит более или менее интенсивное выделение из него ранее поглощенных газов. Это явление называется обезгаживанием тела. Обезгаживание быстро протекает при повышенных температурах и в условиях вакуума. Легкие, подвижные газы (водород, гелий) быстро выделяются из твердых тел при обезгаживании.
Газ может находиться в молекулярном, атомарном и ионизированном состоянии. Наиболее устойчивое состояние газа — молекулярное. Газ в атомарном состоянии неустойчив, а его реакционная способность высока (за исключением инертных газов). Еще более неустойчиво ионизированное состояние газа, в которое он переводится при электрическом разряде во многих газоразрядных лампах.
Таблица 1.7. Свойства технологических газов
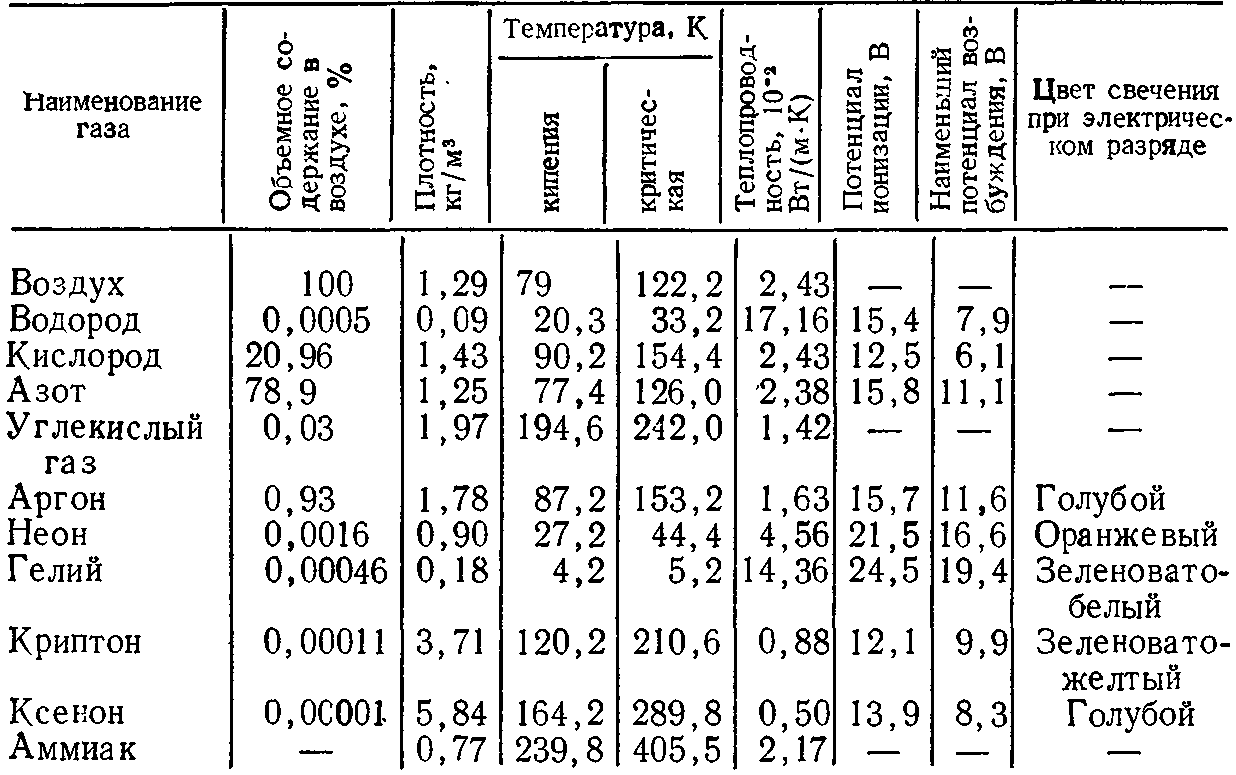
Ионизация газа обычно сопровождается световыми явлениями.
Способность отдельных газов к ионизации и излучению света характеризуется потенциалами ионизации и возбуждения.
Основные свойства технологических газов даны в табл. 1.7.
Получение технологических газов
Получение различных технологических газов может вестись следующими способами: химическими, электрохимическими, разделением воздуха при его глубоком охлаждении и путем их извлечения из газоносных месторождений.
Рис. 1.4. Ячейка электролизера:
1 — изолирующие прокладки; 2 — газовый канал; 3 — газоотводная трубка; 4 — выносной перфорированный катод; 5 — выносной перфорированный анод; 6 — разделительная стенка (электрод); 7 — асбестовая диафрагма; 8 — элемент крепления; 9 — рама
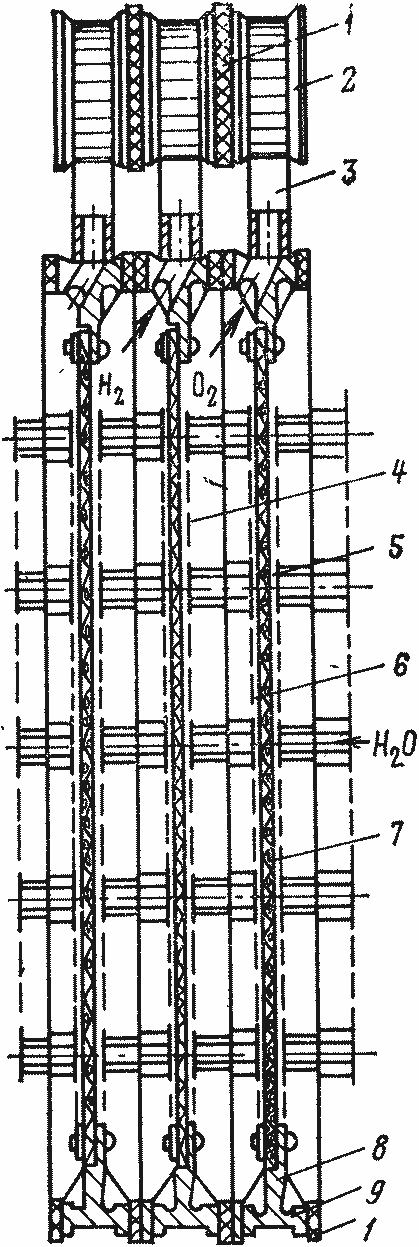
При прохождении постоянного тока через электролит молекулы воды разлагаются на разноименно заряженные ионы, которые под действием электрического поля приобретают направленное движение: ионы Н+ — к катоду, а ионы ОН- — к аноду. На электродах происходит их нейтрализация (разрядка) и образование молекул нейтральных газов: у катода — водорода, а у анода — кислорода. При этом водорода по объему выделяется в два раза больше, чем кислорода.
Для того чтобы в ячейке не происходило смешивания водорода с кислородом (эта смесь взрывоопасна), ее разделяют на две части перегородкой (диафрагмой) из плотного асбестового полотна. Через нее легко проходят ионы Н+ и ОН-, но совершенно не проходят нейтральные молекулы газов водорода и кислорода. Полученные газы отводятся из ячеек электролизера по отдельным трубкам и очищаются от нежелательных примесей (рис. 1.5).
На электроламповых заводах применяются электролизные установки типов Ф24/12, СЭУ-40 и др. Достоинством электролизного способа получения водорода является высокая чистота газа, а недостатком — большие затраты электроэнергии. Так, электролизер типа ЭФ24/12 с производительностью 24 м3/ч по водороду и соответственно 12м3/ч по кислороду потребляет примерно 144 кВт-ч электроэнергии.
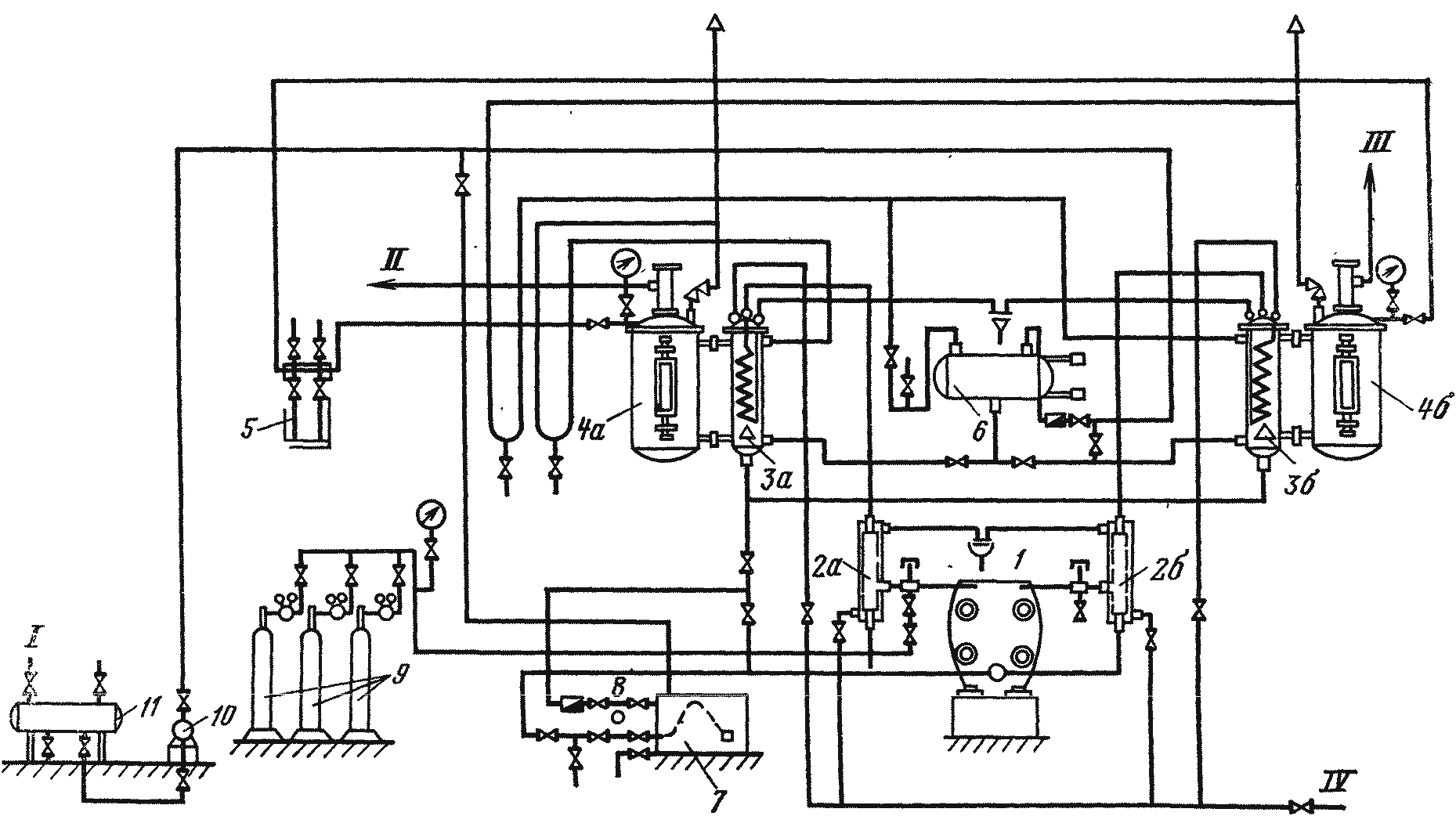
Рис. 1.5. Схема электролизной установки:
1 — электролизер; 2а — разделительная колонка для водорода; 2б — разделительная колонка для кислорода; 3а — промыватель водорода; 3б — промыватель кислорода; 4а — регулятор давления на линии водорода; 4б — регулятор давления на линии кислорода; 5 — дифференциальный манометр; 6 — уравнительная емкость; 7 — сборник электролита; 8 — насос для электролита; 9 —азотная рампа; 10 — насос для дистиллированной воды; 11 — сборник дистиллированной воды; I — дистиллированная вода; II — водород; III — кислород; IV — вода
Производство газов из воздуха. Из воздуха получают кислород, азот, аргон, криптон, неон и ксенон. Процесс получения газов складывается из нескольких этапов — сжижения воздуха, ректификации и очистки.
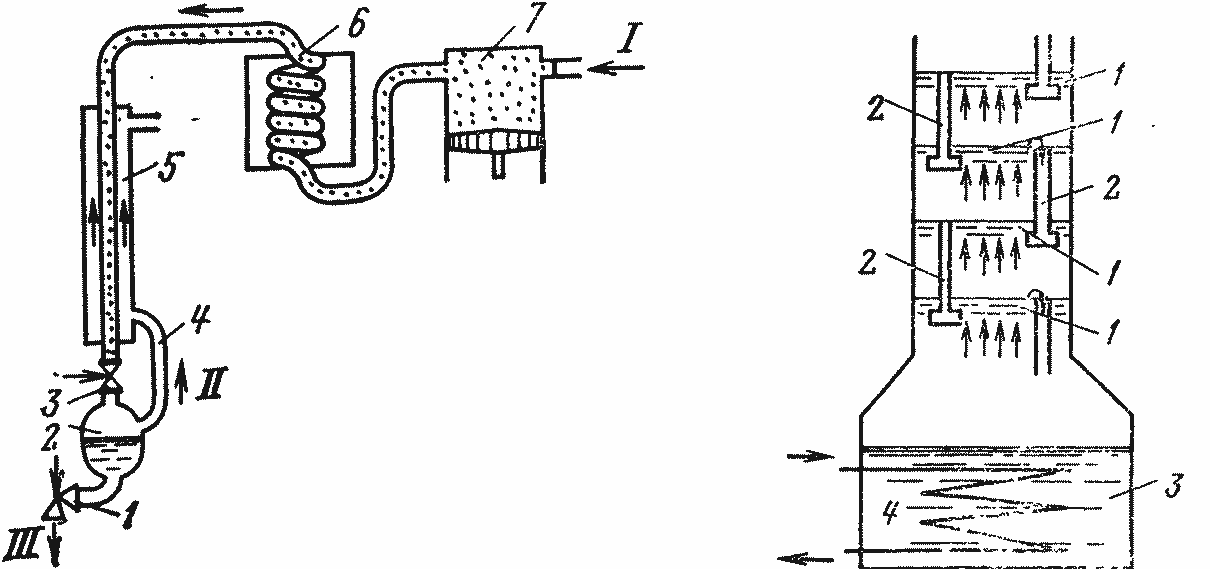
Рис. 1.6. Сжижение воздуха по методу простого дросселирования:
I — атмосферный воздух; II — противоточный пар сжиженного воздуха; III — жидкий воздух; 1 — вентиль; 2 — сосуд с жидким воздухом; 3 —дроссель; 4 — трубопровод; 5 — противоточный теплообменник; 6 — водяной холодильник; 7 — компрессор
Рис. 1.7. Ректификационная колонка:
1 — сетки; 2 — переливные трубки; 3 — испаритель; 4 — змеевик испарителя
Сжижение воздуха основано на его свойстве переходить при глубоком охлаждении из газообразного состояния в жидкое. В промышленных установках (рис. 1.6) профильтрованный атмосферный воздух сжимается компрессором 7 примерно до 20 МПа и подается в первый холодильник 6, где охлаждается проточной водой. Затем сжатый воздух проходит противоточный теплообменник 5, в котором его охлаждение ведется парами ранее сжиженного воздуха. В результате этого температура сжатого воздуха понижается до —140 °C. С целью дальнейшего понижения его температуры сжатый охлажденный воздух пропускают через специальный дроссельный вентиль, имеющий узкий пропускной канал 3. Резкий перепад давлений (с 20 МПа до атмосферного) при выходе воздуха из дросселя, его резкое расширение вызывают понижение температуры воздуха до —196°С. При этом воздух сжижается и собирается в отдельном сосуде 2.
Ректификация представляет собой разделение жидкого воздуха на составляющие фракции, основанное на различии температур кипения и испарения этих фракций — газов, входящих в состав воздуха. Когда воздух кипит, вначале в большей мере испаряются последовательно те газы, температура кипения которых ниже. Аппараты, в которых ведется ректификация жидкого воздуха, называются ректификационными колоннами (рис. 1.7). Наиболее просто получаются кислород и азот.
Для получения инертных газов, процентное содержание которых в воздухе мало, применяют довольно сложную систему многократной ректификации с очисткой требуемого газа от примесей с помощью различных поглотителей.
Из газоносных месторождений добывают только один технологический газ — гелий. При этом гелий получают в качестве попутного (примесного) газа, содержащегося в основных добываемых газах в пределах 1—4% по объему. Разработан процесс отбензинивания нефтяных газов при охлаждении до умеренно низких температур с одновременным отделением тяжелых углеводородов. Оставшийся газ служит сырьем для получения чистого гелия.
Производство газовых смесей.
В электроламповой промышленности широко используется очищенная смесь азота и водорода (последнего 25—75% по объему), известная под названием препарировочного газа или формир-газа. Эта, смесь используется как заменитель чистого водорода на многих технологических операциях из-за ее относительной дешевизны по сравнению с чистым водородом.
Получение препарировочного газа ведется двумя способами: прямым смешением водорода с азотом и разложением аммиака — этот способ более прост и экономичен.
Принципиальная схема установки для получения препарировочного газа прямым смешением показана на рис. 1.8, а.
В смеситель под давлением 0,1—0,3 МПа подводят водород и азот. Процентное содержание газов в смеси регулируется их подачей через вентили с контролем по манометрам. Из смесителя 4 газ поступает в электрическую печь с нагретой восстановленной медью для очистки от кислорода, далее через холодильник 7 с проточной водой для конденсации водяного пара в бачок с кусковой щелочью 8, где поглощается углекислый газ и происходит более тщательная очистка от водяного пара. Показанные на рисунке буферные бачки 5 сглаживают возможные колебания давления газа в установке.
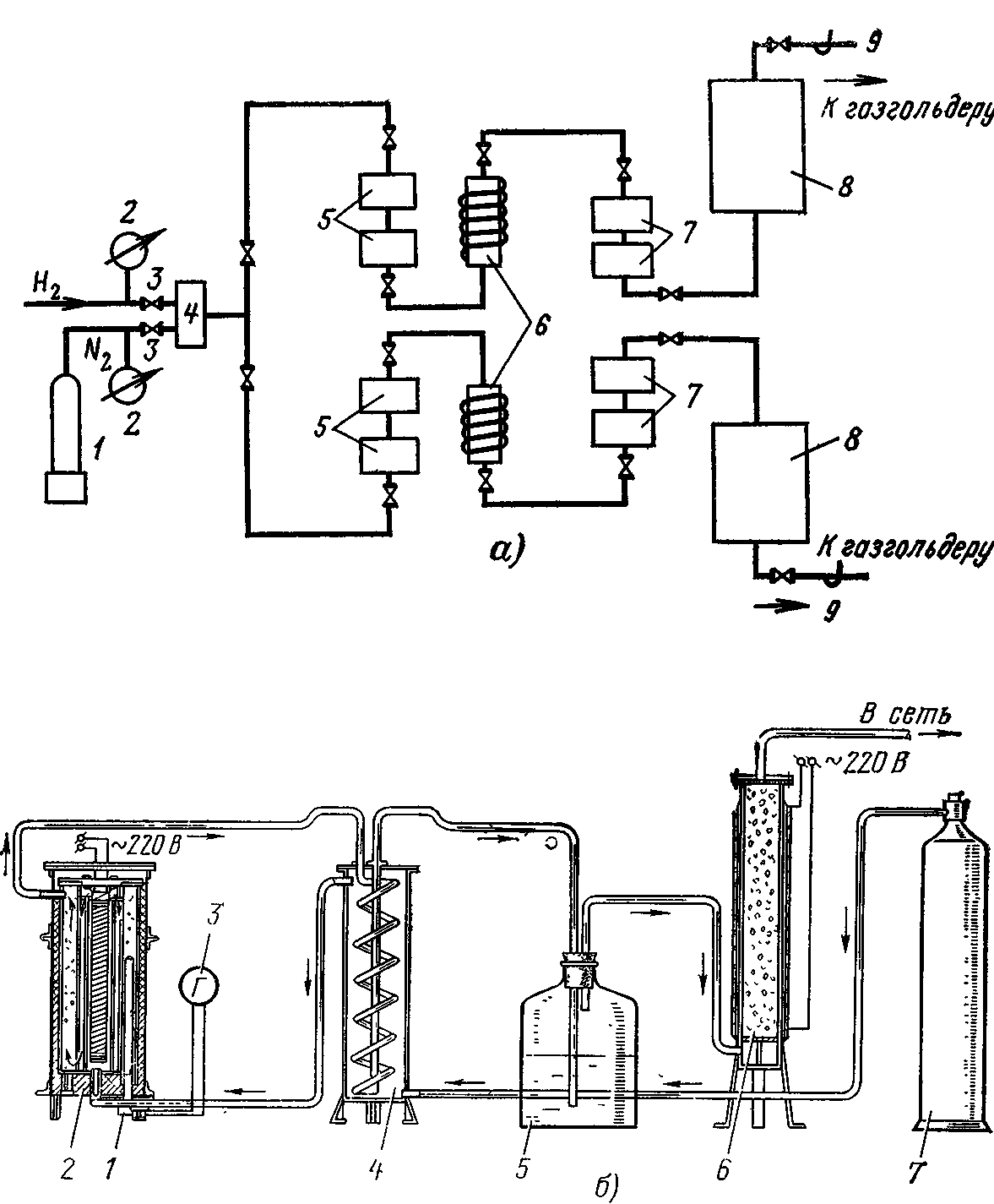
Рис. 1.8. Схемы установок получения препарировочного газа:
а — смешением (1 — баллон с азотом; 2 — манометры; 3 — клапаны; 4 — смеситель; 5 — буферные бачки; 6 — печи поглощения водорода; 7 — холодильники; 8 — бачки со щелочью; 9 — манометры); б — разложением аммиака (1 — термопара; 2 — печь разложения аммиака; 3 — гальванометр; 4 — теплообменник; 5 — бутыль с раствором серной кислоты; 6 — сосуд с силикагелем; 7 — баллон с жидким аммиаком)
Для обеспечения непрерывности работы смесительную установку обычно собирают из двух параллельных ветвей, одна из которых находится в рабочем состоянии, а другая — на регенерации. Затем они периодически переключаются. На выходе газ может иметь давление 13—40 кПа.
Принципиальная схема установки для получения препарировочного газа разложением аммиака показана на рис. 1.8,б.
Жидкий аммиак под давлением 0,7—0,8 МПа поступает из баллона в теплообменник 4, где, нагреваясь, переходит в газообразное состояние. Газообразный аммиак подается в электрическую печь 2 с катализатором (окисленная стальная стружка или покрытие окисью железа керамические шарики). Проходя через нагретый до 1000—1050 К катализатор, аммиак разлагается на азот и водород
2ΝΗ3=3Η2+Ν2. (1.3)
Полученная смесь очищается от остатков неразложившегося аммиака в сосуде с 20%-ным раствором серной кислоты 5, осушивается пропусканием через силикагель и активированный уголь 6 и поступает в газопровод. Точка росы осушенного газа должна быть не выше —20 °C. Из 1 кг сжиженного аммиака получается газовая смесь 650 л азота и 1950 л водорода.
Другие газовые смеси получают обычно методом прямого смешения соответствующих газов.
Очистка технологических газов.
К технологическим газам часто предъявляют жесткие требования по чистоте. Основными загрязняющими примесями могут быть: механические-частицы (пыль, капли масел и др), влага, углекислота, другие газы, отличающиеся от основного. В зависимости от вида загрязняющей примеси, рода основного газа, необходимой степени очистки применяют различные способы очистки.
- Очистка от влаги. Необходимая степень осушки газов может быть достигнута следующими способами: вымораживанием паров воды путем пропускания загрязненного газа через трубопровод с охлажденным участком; с помощью гигроскопических веществ (фосфорный ангидрид Р2О5, едкое кали КОН, едкий натр NaOH, негашеная известь СаО, силикагель SiO2-H2O, алюмогель АlО3-Н2О и др.); с помощью цеолитов («молекулярных сит»); путем пропускания газа через сосуд с крепким этиловым спиртом.
Весьма эффективна осушка газа при комбинации различных способов, например, в следующей последовательности: вымораживание при охлаждении жидким азотом, осушка с помощью силикагеля, осушка с помощью фосфорного ангидрида.
Иногда ставится задача не осушать, а увлажнять газ. Для этого его пропускают пузырьками через сосуд с подогретой дистиллированной водой. Содержание паров воды в газе обычно оценивается точкой росы, т. е. температурой, до которой надо охладить газ, чтобы содержащийся в нем водяной пар стал насыщенным и начал конденсироваться в виде росы.
D производстве источников света применяют как увлажненные газы (например, с точкой росы 0—20°C), так и высоко-осушенные газы (например, с точкой росы от —60 до -50 °C).
- Очистка от примесей кислорода. Для очистки газа от примесей кислорода применяют железо-медно-никелевые катализаторы, чистую восстановленную медь в виде стружки или губчатую медь. Оптимальная температура 300—350 °C. Очистка достигается за счет связывания свободного кислорода нагретым катализатором. Например, в случае применения меди имеет место реакция
![]() (1-4)
(1-4)
- Очистка от углекислоты. Очистка от углекислоты СО2 ведется пропусканием газа через бачок с кусковой щелочью.
- Очистка газа от водорода и окиси углерода. Для очистки газа от водорода и окиси углерода его пропускают над нагретой до 300—350 °C окисью меди
![]() (1-5)
(1-5)
Продукты восстановления окиси меди — пары воды и углекислый газ выводятся из печи вместе с газом, а затем отделяются от него рассмотренными выше способами.
- Очистка от углеводородов. Очистка от углеводородов ведется также пропусканием загрязненного газа над окисью меди, но нагретой до более высокой температуры — около 700—770 °C. Например, для метана имеет место реакция
![]() (1-6)
(1-6)
Для очистки газа от органических загрязнений иногда вместо высокотемпературной печи с окисью меди устанавливают печь с керамическими кольцами, пропитанными металлическим палладием. В присутствии палладиевого катализатора облегчаются реакции между водородом, окисью углерода и углеводородами, с одной стороны, и кислородом — с другой, даже при относительно низких температурах.
- Очистка от механических частиц. От механических частиц газ очищается пропусканием через стекловату или тканевые фильтры. В реальных условиях приходится очищать газ от многих видов примесей, пропуская его через сложные системы очистки. Схема одной из таких систем очистка азота и аргона показана на рис. 1.9.
Производительность газоочистительной системы при среднем содержании кислорода в неочищенном газе до 4 л/м3 составлю ет 2 м3/ч.
По техническим требованиям электроламповых заводов объемное содержание кислорода в техническом азоте не должно превышать 0,5%, а в техническом аргоне — 0,4%, содержание углекислого газа в азоте и аргоне не должно превышать 0,3%, сернистого газа и углеводородных соединений в аргоне не должно быть совсем.

Рис. 1.9. Система очистки азота и аргона:
1 —баллон с неочищенным газом; 2 — редукционный вентиль с манометрами низкого и высокого· давления; 3, 8 — бачки со щелочью; 4 — печь с окисью меди (650—750 °C); 5 — печи с металлической медью (300—350 °C); 6 — печи с окисью меди (300—350 °C), 7 — холодильник; 9 — бачок с натровой известью; 10 — детандер; 11 — сосуды с фосфором; 12 — манометры; 13 — ловушка со стекловатой; 14 — краны; 15 — индикаторная лампа; 16 — клапаны
После дополнительной очистки содержание нежелательных примесей в технологических газах может быть очень малым. Так, в аргоне особой чистоты аргона должно быть не менее 99,994% по объему, азота не более 0,005% и кислорода не более 0,001%.
Качественную оценку степени чистоты газа производят индикаторными лампами накаливания, вмонтированными в газоочистительную систему.
Точный количественный анализ состава газов проводится в лабораториях электроламповых заводов с использованием довольно сложных газоанализаторов, работа которых может быть основана на адсорбционных, масс-спектрометрических, спектральных и других методах.
б) Топливные газы. Назначение и области применения.
В электроламповой промышленности газ как топливо широко используется для различных технологических процессов: варки стекла, его термической обработки при изготовлении деталей, заварки ламп и т. п.
В качестве топливных используются следующие газы: природный, генераторные, сжиженные и чистый водород. Все эти газы, за исключением водорода, являются обычно смесью нескольких простых горючих газов и примесей к ним. К таким простым горючим газам относятся: водород, метан, этан, пропан, бутан, окись углерода, некоторые тяжелые углеводороды.
Примесными (балластными) газами топлива являются азот, углекислота, водяные пары, сероводород. Чем меньше в топливном газе содержится примесей (балластных, негорючих) газов, тем выше его качество.
Газы, используемые в качестве топлива на Технологических операциях электролампового производства, должны удовлетворять следующим требованиям: иметь достаточно высокую температуру горения; не загрязнять помещения и обрабатываемые детали вредными веществами; иметь постоянный состав, легко очищаться; быть удобными при сжижении и транспортировке; быть дешевыми и доступными и т. п. Большинство из вышеперечисленных топливных газов удовлетворяет этим требованиям.
Свойства.
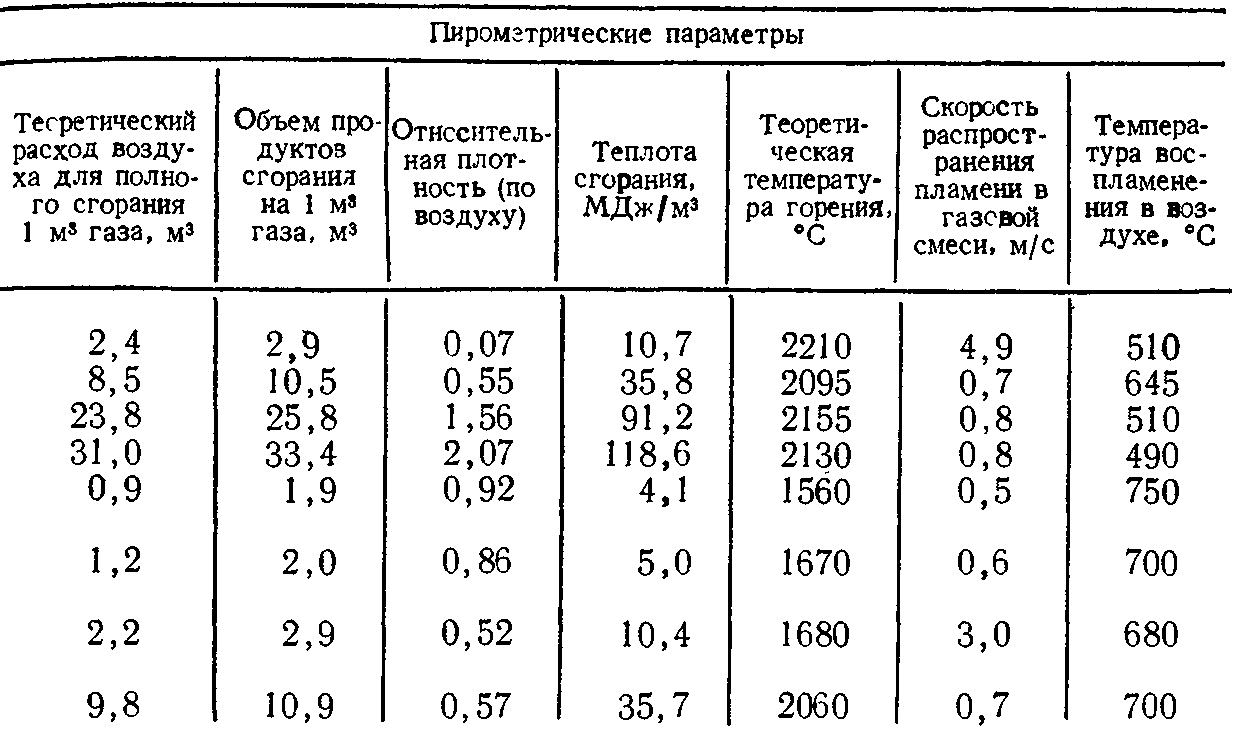
К важнейшим свойствам топливных газов относятся состав, теоретический расход воздуха, необходимого для полного сгорания 1 м3 газа, объем продуктов сгорания 1 м3 газа, относительная плотность (по воздуху), теплота сгорания, теоретическая температура горения, скорость распространения пламени, температура воспламенения в воздухе. Показатели этих свойств приведены в табл. 1.8.
Сжигание газа.
Эффективность любого топливного газа в первую очередь определяется его способностью гореть. Горение — это процесс окисления топлива, сопровождающийся быстрым выделением теплоты и, как правило, света.
Таблица 1.8. Свойства топливных газов

Продуктами горения являются двуокись углерода, пары воды, а также балластные газы, которые непосредственно в процессе горения не участвуют, но могут находиться в топливе в качестве примесей.
Различают кинетическое, диффузное и смешанное горение газа. В кинетическом горении участвуют полностью подготовленная газовоздушная смесь, в диффузном — воздух из окружающей среды и газ, подаваемый через горелку, в смешанном — частично подготовленная газовоздушная смесь из горелки и дополнительно воздух, поступающий из окружающей среды.
В производстве электроламп кинетическое горение газа имеет место в стекловаренных печах и печах отжига (лерах), а диффузное и, главным образом, смешанное — на многочисленных операциях, газопламенной обработки стеклянных деталей ламп.
Сжигание газа может быть полным и неполным. При полном сжигании газа продукты горения состоят только из негорючих газов; факел пламени имеет сине-фиолетовый оттенок за счет люминесценции нагретых газов. При неполном сжигании газа в продуктах горения содержится некоторое количество недогоревших горючих газов; пламя получается непрозрачным, с интенсивным свечением за счет накаленных частиц углерода.
Газовое пламя может обладать окислительными или восстановительными свойствами, обусловленными наличием в избытке соответственно кислорода или водорода и окиси углерода в пламени. Обычно внутренние части пламени обладают восстановительными свойствами, а наружные — окислительными. Химические свойства пламени необходимо учитывать при обработке в нем свинцового стекла, а также при спаивании стекла с металлом. Вид, строение и размеры пламени зависят в основном от состава газа, вида горения и конструкции горелки.
Различают также мягкое, жесткое и среднее пламя. Мягкое пламя — низкотемпературное, получается при диффузном горении. Жесткое пламя — высокотемпературное, получается при интенсивном и полном сжигании газа часто с подачей в горелку кислорода. Смешанное горение газа дает среднее пламя, характеризующееся умеренными температурами и занимающее по температуре горения среднее положение между мягким и жестким пламенем.