Вплив взаємодії атомів і молекул на спектри випромінювання різних речовин
Розглянута в попередньому розділі схема заповнення енергетичних рівнів електронами визначає спектри оптичного випромінювання ізольованих атомів. Вона придатна для газів та парів різних речовин при досить сильному їхньому розрідженні, коли взаємодія атомів та молекул у них надзвичайно мала.
Будь-яке тіло, як газоподібне, так і рідке або тверде, фактично являє собою простір, в якому ніби вкраплена велика кількість електронів і ядер, що утворюють атоми, оскільки розміри цих мікрочастинок дуже малі порівняно з відстанню між ними в атомах. Маса тіл в основному визначається масою ядер їхніх атомів, тому що у електронів вона набагато менша. Об’єм кожного атома визначається розмірами найбільшої орбіти, яка зайнята в атомі його електронами. Отже, простір, зайнятий тілом, заповнюється головним чином не частинками, що його створюють (ядрами та електронами), а електричними полями, які утворюються цими частинками.
Між електронами та ядрами різних атомів і молекул, які створюють будь-яке тіло, виникають електростатичні (кулонівські) сили відштовхування або притягання, тобто різні атоми у тілах взаємодіють між собою. При ущільненні речовини (зближенні молекул) ця взаємодія різко підсилюється, тому що різко зростають кулонівські сили, які діють між зарядами частинок цієї речовини. При цьому електрони різних атомів притягають до себе ядра атомів, які знаходяться поблизу і урівноважують взаємне відштовхування останніх. У результаті, зокрема для металів, вони забезпечують цілісність твердого тіла.
Цілісність молекул і тіл, які вони утворюють, обумовлена і силами іншого роду, зокрема, магнітними та квантово-механічними обмінними силами. Відмінність між агрегатними станами речовин (газ, плазма, рідина, тверде тіло) є наслідком різного характеру взаємодії їхніх атомів і молекул між собою.
Обмінні сили діють тільки у мікросвіті, тобто між мікрочастинками і можуть бути величезними. Проте помітними вони стають лише при зближенні мікрочастинок на такі малі відстані (10-15... 10-10 м), що фактично вони прилягають одна до одної. Тому ці сили іноді називають силами прилипання. Гравітаційні сили порівняно з ними дуже малі. Саме обмінні сили, які значно перевищують електростатичні, міцно утримують у ядрі атома в дуже щільній упаковці позитивно заряджені протони, незважаючи на взаємне дуже сильне відштовхування їхніх зарядів. Називають їх у цьому випадку ядерними силами.
При дуже малій відстані між молекулами обмінні сили можуть утворювати надзвичайно міцні сполучення молекул між собою, як, наприклад, в алмазах. Між молекулами газів та парів обмінні сили не діють через недостатню для їхнього виникнення близькість молекул.
Наслідками взаємного впливу атомів у тілах є зміна енергії дозволених рівнів електронів при зближенні атомів, а також зміна відстаней між цими рівнями. В результаті дозволені енергетичні рівні, які майже зливались в ізольованих атомах, при зближенні атомів розсовуються (розщеплюються), що фактично еквівалентно виникненню нових можливих збуджених станів атомів. Схематично це зображено на рис. 1.8, де по вертикальній лінії відкладають значення енергії електронів у атомі, а по горизонтальній - відстань між атомами d. Наведені графіки відповідають двом першим квантовим станам атома (п= 1 і ml=0; п = 2 і ml=0).
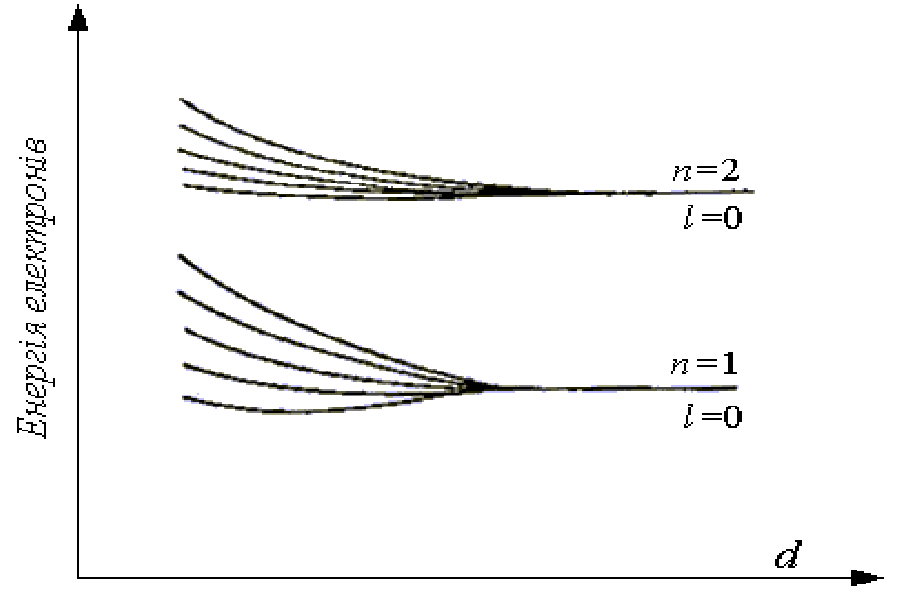
Рис. 1.8. Вплив взаємодії атомів на енергетичні рівні їхніх електронів
При великій кількості близько розташованих атомів число розщеплених енергетичних рівнів, які помітно відрізняються енергією, також стає великим. Відбувається взаємне проникнення електронів одного атома на орбіти іншого. У газі відстані між атомами дуже залежать від його тиску. У рідинах, а особливо в твердих тілах сили взаємодії між атомами набагато більші, ніж у газах. Тому кількість проміжних дозволених енергетичних рівнів для електронів в атомах рідин і твердих тіл більша, ніж у газів. Відповідно відстані між дозволеними енергетичними рівнями у них можуть бути дуже малими. При цьому слід зазначити, що для виникнення світлових променів та променів з довжинами хвиль, близькими до довжин хвиль світлових променів, найбільше значення має розщеплення енергетичних рівнів у валентній зоні атомів.
У металах у твердому стані взаємодія атомів стає настільки сильною, що для валентних електронів розподіл дозволених рівнів стає майже неперервним. Відповідно спектри випромінювання металів у твердому стані стають майже суцільними.
В атомарних газах і парах при їхньому ущільненні відокремлені спектральні лінії розширюються. При дуже великій густині газоподібних речовин, коли взаємодія атомів при їхньому зближенні значно зростає, спектри випромінювання таких речовин стають значно розширеними. Проте суцільні спектри випромінювання можуть мати лише тіла, які знаходяться у твердому або рідкому станах.
Приблизна схема енергетичних рівнів для одного ізольованого атома міді показана на рис. 1.9,а, а на рис. 1.9,б - для великої кількості таких атомів у кристалічному твердому тілі.
Дозволені рівні на рис. 1.9,а зображені горизонтальними лініями. Електрони, які знаходяться на декількох нижніх дозволених рівнях, як і вище, умовно зображені кружечками.
Через те, що поза атомом можливі будь-які значення енергії електронів, дозволені рівні енергії для електронів у цій області слідують неперервно. Ця область показана на рис. 1.9,а у верхній його частині.
Взаємний вплив атомів міді, які знаходяться у кристалічному твердому тілі, призводить до того, що дискретні дозволені енергетичні рівні електронів розщеплюються у смуги (зони) з квазінеперервною послідовністю дозволених значень енергії в межах кожної смуги. Дозволені енергетичні зони, заповнені електронами, на рис. 1.9,б зображені у вигляді чорних смуг, а вільні зони - заштриховані. Заборонені зони на цьому рисунку залишені білими.
Рис. 1.9. Схема енергетичних рівнів одного ізольованого атома міді (а) та великої кількості таких атомів у твердому тілі (б)
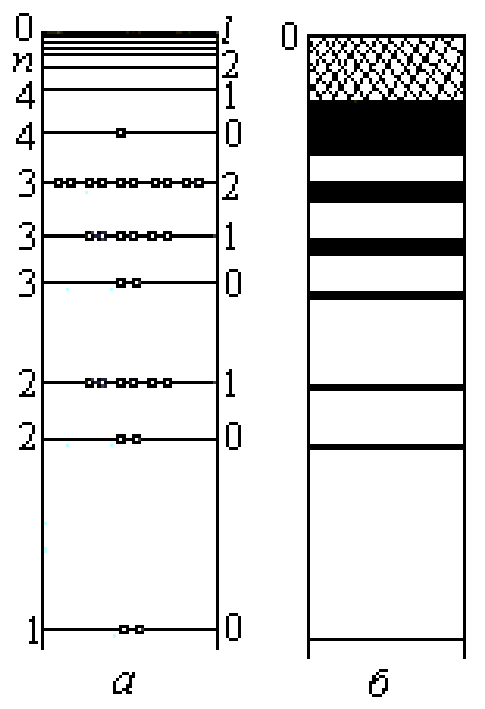
З рис. 1.9,б ясно видно, що найсильнішим є розщеплення енергетичних рівнів валентних електронів і більш високих вільних рівнів.
У той час, коли окремий ізольований атом може отримувати енергію лише у вигляді енергії збудження, що призводить до електронних переходів, атоми і молекули у структурі тіл можуть отримувати енергію й іншими способами. У нормальному (сталому) стані вони знаходяться у тілах в таких положеннях, в яких повна енергія системи знижується до мінімальної. При отриманні додаткової (надмірної) енергії, тобто при збудженні вони можуть почати обертатися навколо якоїсь осі або їхні ядра будуть коливатися відносно одне одного.
У результаті передачі енергії молекулам іззовні можуть також відбуватися зміщення атомів з їхніх рівноважних положень в молекулах, обертання одних частин молекули відносно інших і можуть виникати електронні переходи в їхніх атомах, пов’язані з коливаннями атомів у молекулах відносно своїх рівноважних положень і т. ін.
Як обертання атомів і молекул в структурі тіла, так і коливання ядер відносно одне одного та зміщення атомів у молекулах підпорядковуються усім законам квантової механіки, тобто надмірна енергія може передаватися атомам і молекулам і у цих випадках лише певними порціями. Проте енергетичні рівні при подібних збудженнях розташовуються дуже щільно.
При поверненні атомів і молекул зі збуджених станів, які викликані кожним з названих вище збуджень, у нормальний (сталий) зайва енергія випромінюється у вигляді квантів. У результаті у спектрах випромінювання тіл з’являються характерні лінії або їхня сукупність, яких немає в спектрах випромінювання окремих ізольованих атомів цих тіл (коливальні, обертальні, електронно- коливальні та інші спектри молекул).
Обертання молекул призводить до “розмиття” ліній спектрів випромінювання в смуги, через що вони набувають характерної лінійчасто-смугастої структури.
Теплове збудження зв’язаних часток твердих тіл відбувається в основному як коливання цих часток відносно вузлів кристалічної гратки.